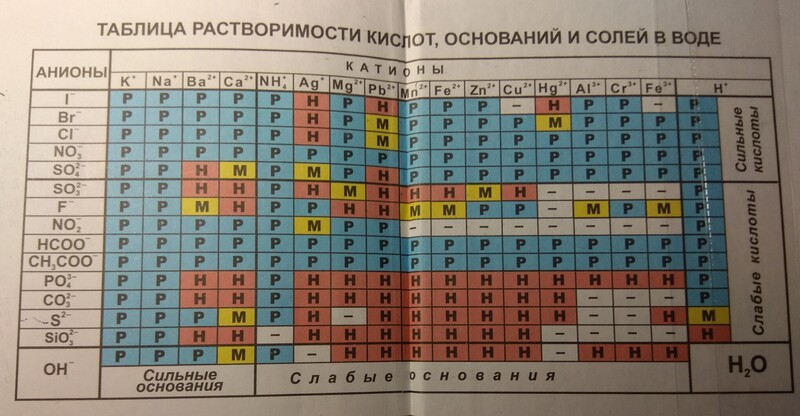
Растворимость – это способность одного вещества взаимодействовать с другими веществами, образуя при этом однородные растворы.
На сегодняшний день существует таблица способная помочь в определении растворимости химического соединения.
Чтобы пользоваться таблицей не обязательно иметь специальных навыков. Для определения растворимости какого-либо химического вещества, достаточно в таблице провести перпендикуляр от выбранного вещества начиная от крайней левой колонки до химического вещества в верхней колонке. Точка пересечения и укажет нам насколько растворимы выбранные вещества.
Рассмотрим на примере, как пользоваться таблицей растворимости солей, кислот и оснований:
В левой колонке выберем вещество Ba2+, проводим линию до 3-й колонки с веществом F-, на пересечении видим символы «РК». Это означает, что соединение нерастворимо в воде и растворяется только в сильных неорганических кислотах.
Таблица условных обозначений
| Р | растворимо в воде (больше 1 грамма вещества на 100 грамм воды) |
| М | малорастворимо в воде (от 0,001 грамма до 1 грамма вещества в 100 граммах воды) |
| Н | нерастворимо в воде, но хорошо растворимо в слабых кислотах (меньше 0,001 грамма до 1 грамма вещества в 100 граммах воды) |
| РК | нерастворимо в воде, но растворимо в сильных неорганических кислотах |
| НК | химическое вещество не растворимо ни в воде, ни в любых кислотах |
| Г | химическое вещество подвергается гидролизу |
| - | данные о растворимости химического вещества отсутствуют |
Таблица растворимости солей, кислот и оснований по химии
| Катионы |
Анионы | ||||||||||
| OH- | F- | Cl- | Br- | I- | S2- | NO3- | CO32- | SiO32- | SO42- | PO43- | |
| H+ | Р | Р | Р | Р | Р | М | Р | - | Н | Р | Р |
| Na+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| K+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| NH4+ | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р |
| Mg2+ | Н | РК | Р | Р | Р | М | Р | Н | РК | Р | РК |
| Ca2+ | М | НК | Р | Р | Р | М | Р | Н | РК | М | РК |
| Sr2+ | М | НК | Р | Р | Р | Р | Р | Н | РК | РК | РК |
| Ba2+ | Р | РК | Р | Р | Р | Р | Р | Н | РК | НК | РК |
| Sn2+ | Н | Р | Р | Р | М | РК | Р | Н | Н | Р | Н |
| Pb2+ | Н | Н | М | М | М | РК | Р | Н | Н | Н | Н |
| Al3+ | Н | М | Р | Р | Р | Г | Р | Г | НК | Р | РК |
| Cr3+ | Н | Р | Р | Р | Р | Г | Р | Г | Н | Р | РК |
| Mn2+ | Н | Р | Р | Р | Р | Н | Р | Н | Н | Р | Н |
| Fe2+ | Н | М | Р | Р | Р | Н | Р | Н | Н | Р | Н |
| Fe3+ | Н | Р | Р | Р | - | - | Р | Г | Н | Р | РК |
| Co2+ | Н | М | Р | Р | Р | Н | Р | Н | Н | Р | Н |
| Ni2+ | Н | М | Р | Р | Р | РК | Р | Н | Н | Р | Н |
| Cu2+ | Н | М | Р | Р | - | Н | Р | Н | Н | Р | Н |
| Zn2+ | Н | М | Р | Р | Р | РК | Р | Н | Н | Р | Н |
| Cd2+ | Н | Р | Р | Р | Р | РК | Р | Н | Н | Р | Н |
| Hg2+ | Н | Р | Р | М | НК | НК | Р | Н | Н | Р | Н |
| Hg22+ | Н | Р | НК | НК | НК | РК | Р | Н | Н | М | Н |
| Ag+ | Н | Р | НК | НК | НК | НК | Р | Н | Н | М | Н |